药物渗漏是指抗癌药物浸润、渗漏到血管外部的现象。外渗可能会损坏周围的软组织,导致发红,肿胀,疼痛,灼热,糜烂,起泡,溃疡和坏死等。严重时可能长期无法恢复,影响患者的QOL。预防渗漏和及时纠正至关重要。
症状和过程
注射抗癌药物发生渗漏时有几种情况:1)没有出现任何症状;2)有发红,肿胀,疼痛,灼热感;3)数小时或数天后症状恶化,经历水泡-溃疡-坏死的过程。多数溃疡很难治疗,泄漏的部位可能出现疤痕挛缩,将来活动受限,有时甚至需要手术干预。例如,注射紫杉醇或多西他赛时发生了渗漏,尽管渗出的部位得到了恢复,但再次注射同药物时先前渗出的部位仍可能出现皮肤症状。
风险因素
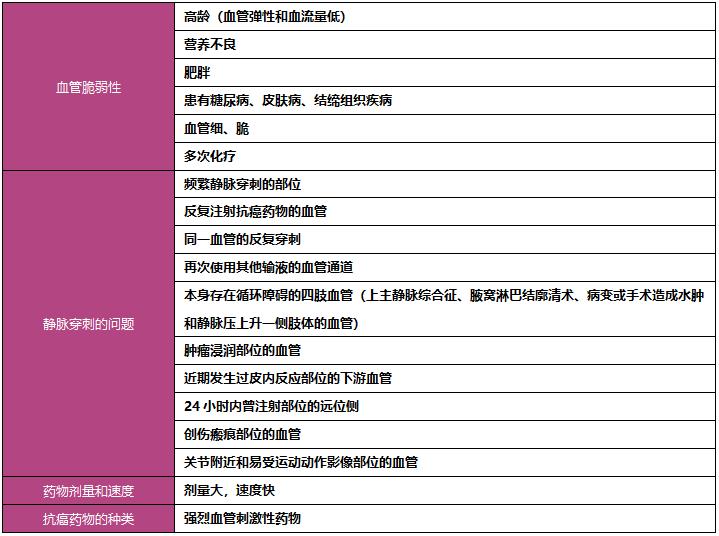
表1显示了抗癌药物泄露的危险因素。有文献报道化疗时药物渗出的频率约为0.5%~6.5%。所有抗癌药物均可能通过外渗引起局部坏死。风险因素越多,渗漏的风险也越高。使用易引起坏死的抗癌药物时,有必要在开始治疗之前对患者进行评估。
表1:血管渗漏的风险因素
Grade评级
以CTCAEv5.0版本为基础。
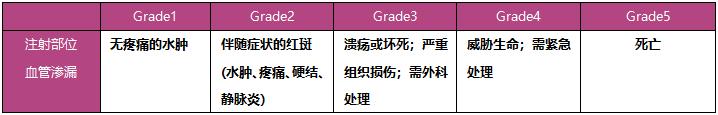
表2:注射部位血管渗漏的Grade评级
抗癌药物的分类
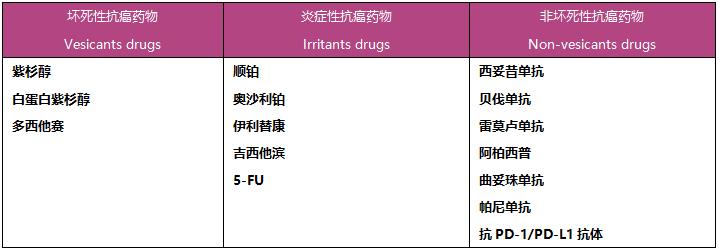
不同的抗癌药物对皮肤组织的损伤程度不同,按危险程度分为坏死性药物,炎症性药物和非坏死性药物三大类。
坏死性抗癌药物(vesicants drugs)
少量的血管渗漏即可能造成发红,肿胀,疼痛,坏死或顽固性溃疡。坏死性抗癌药物分为DNA结合型和非DNA结合型,应特别注意DNA结合型。血管外渗对组织的损伤不仅与药物的种类有关,还与剂量、浓度、渗出量、暴露时间有关,需要综合评估。
炎性抗癌药物(irritants drugs)
可造成局部发红、肿胀,但不导致溃疡的抗癌药物。但血管外渗量过多时也发生溃疡。
非坏死性药物(non-vesicants drugs)
即使发生外渗也不太可能引起炎症和坏死的抗癌药物。
表3:血管外渗的组织伤害性分类(消化道领域)
对策
即使少量的血管外渗也可能导致坏死、溃疡等顽固性皮肤损害,有必要熟悉预防措施和快速处理方法。
预防
关于抗癌药物的血管渗漏,本身有规范的化疗护理指南、欧洲肿瘤护理学会(EONS)指南等。按照指南或更严格的院内规则操作,能最大限度地降低外渗风险。预防要点如下:
①勿使用超过24小时以上的外周静脉管线。
②选择粗壮且未受损的血管。第一选择部位是前臂,避免手背和肘关节附近穿刺。如果难以确定路线,加热手臂以扩张血管。
③输液前确认有回血。给药前用生理盐水冲管以确认没有泄漏。
④固定输液路线,使用透明胶带可观察到刺入部位。
⑤输液结束时,用生理盐水冲管,并压迫止血。
⑥穿刺失败后再穿刺时,选择对侧血管或同侧中枢血管。
⑦穿刺困难的考虑留置CV端口。
治疗
当发生外渗时,立即处置以减少暴露剂量和时间。尽可能清理外渗药物,对患处进行治疗(冷却、加热、局部使用激素等),进行随访观察,必要时考虑外科处理。血管外渗的处理要点:
①立即停止静脉滴注。
②吸引留置针内和外渗的残留药液,然后取出针头。
③根据抗癌药物的种类妥当处置。
坏死性抗癌药物/炎症性抗癌药物
・蒽环类药物泄漏时给予右雷佐生注射
・局部注射激素(+局部麻醉)
・局部涂抹外用激素
・局部冷却
・处置后持续局部冷却和涂抹激素
非坏死抗癌药物
・改变注射部位
・大范围泄漏时进行冷却处理
④对事件进行记录。
⑤随访观察。必要时咨询皮肤科和整形外科医师。
冷却和加温
如发生药物外漏通常推荐冷却处理。冷却收缩局部血管,将药物控制在局部,同时也希望冷却能降低抗癌药物的活性。
有文献认为长春碱类化合物外渗经冷却后可能造成溃疡的恶化。推荐此类药物外渗时采用加热方式处置,加热能扩张泄漏部位血管,增加血流量从而扩散和稀释药物。奥沙利铂外渗后不推荐冷却,因为降温会诱发或加剧急性神经疾病。
局部注射激素
发生血管外渗后,推荐使用地塞米松、倍他米松、泼尼松龙、可的松等激素,混合麻醉剂局部注射,注射范围大于泄漏部位。期待局部注射激素发挥抗炎作用,但尚未证明它们足够有效,未达到临床推荐水平。
解毒药剂
部分国家的药监部门批准用右雷佐生治疗蒽环类抗癌药物的血管外渗。推荐发生药物渗出后的6小时内尽快开始使用右雷佐生解毒,并持续治疗3天(第1天和第2天为1,000 mg / m2,第3天为500 mg / m2)。
表4:药物外渗时的解毒药物(临床效果不明确)
管理要点
抗癌药物的外渗会导致溃疡和坏死等顽固性皮肤疾病,对患者的生活质量产生重大影响。应重视点滴前的风险评估和预防。点滴过程中注意观察以尽早发现外渗,发生外渗时迅速妥当处置。外渗的第一个发现者往往是患者,在点滴前患者和家属应了解药物外渗的知识,意识到尽早报告异常情况。