2019年6月18日,罗氏宣布,日本厚生劳动省(MHLW)已批准Rozlytrek®(entrectinib,恩曲替尼)用于治疗神经营养性酪氨酸受体激酶(NTRK)融合阳性的晚期复发性实体瘤的成人和儿童患者。
相信仔细看过邱医生前段时间文章的小伙伴们对于恩曲替尼并不陌生,但是这个“NTRK”到底是什么东东?估计很多人都不知道了。那么今天,邱医生就来接着跟大家聊聊靶向治疗中的--NTRK。
NTRK身份证
NTRK基因家族包含NTRK1、NTRK2和NTRK3,分别代表染色体上三个不同的基因位点。正常情况下他们各司其职,其中:NTRK1基因编码TRKA,与神经营养因子(NGF结合);NTRK2基因编码TRKB,与脑源性神经营养因子(BDNF)和神经营养因子4(NT-4)结合;NTRK3基因编码TRKC,与神经营养因子3(NT-3)结合。
和前面介绍过的其他基因一样,如果任何一个位点的基因和其他的基因发生了融合突变,那么就会导致下游信号通路的异常,进一步的后果就是会驱动肿瘤的发生,目前3个基因融合导致的3个TRK受体结构激活被认为是实体肿瘤(包括肺癌、唾液腺癌、甲状腺癌和肉瘤)的致癌因素。
简单了解了NTRK是个什么东东,接下来一起来看看它在各个实体肿瘤中的突变频率吧
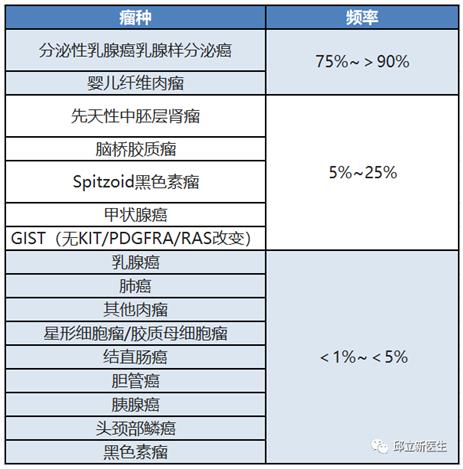
可以看出,虽然NTRK是个济济无名的家伙,但是由于各种原因不幸发生突变的它们其实有可能正默默地在很多地方捣蛋呢。
此前,在肺癌领域为大家所熟知的靶向用药基因主要有8个,即:EGFR、KRAS、HER2、ALK、ROS1、MET、BRAF 和 RET。在2019年1月18日公布的NCCN非小细胞肺癌指南中,新增了一个NTRK基因融合,由此开始,肺癌领域的靶向用药基因由8个变成了9个。
(在肺癌领域,最常见的是 TPR-NTRK1融合。NSCLC 的患者中有 0.2% 存在 NTRK 融合,通常不与其它致癌驱动因子同时存在,如 :EGFR、ALK或ROS1。)
至此,NTRK基因融合可算是小小的“扬眉吐气”一把。
可是,话说回来,就算在肺癌领域国外指南有写它,但实际上在不同瘤种中,这个基因突变频率不尽相同,而且目前国内的研究也不多,近期也没听说有什么针对性药物在国内上市。对于我们普通小老百姓而言,了解它、检测它有什么用?是不是浪费钱?想知道答案,您请往下看~~~
可别小看我NTRK,虽然目前在国内暂时还没啥大动静,但是在国外,早已是研究得如火如荼呢
“抗癌神药”--拉罗替尼(Larotrectinib、Vitrakvi)
拉罗替尼是由Loxo Oncology和拜耳(Bayer)公司共同开发,又名Vitrakvi(larotrectinib,代号 Loxo101)。它是第一个针对NTRK 基因融合突变的、口服的、广谱靶向药。该药的最大看点在于,它是一款针对特定基因突变(NTRK 基因融合突变),而不针对特定癌症种类的抗癌新药。于2018年11月12日,FDA加速批准上市,用于治疗携带NTRK基因融合的成年和儿童局部晚期或转移性实体瘤患者,不需考虑癌症的发生区域。
您看到重点了吗?
适应症中的“成年和儿童”、“不需考虑癌症的发生区域”,这意味着,相较于目前市面上的其他抗肿瘤靶向药物而言,拉罗替尼相对安全性较好,而且针对不同癌种有效率均很高。
此前FDA公布数据显示,73%的患者反应时间为6个月以上,63%的患者反应时间为9个月以上,39%的患者反应时间为12个月以上。2018年2月,世界四大权威医学杂志之一《新英格兰医学杂志(NEJM )》发表的一项关于larotrectinib的3项安全性和有效性临床研究结果显示:对于年龄为4个月至76岁的患者,针对17种不同癌症治疗的总体有效率为75%。这项结果随后也被FDA所证实。紧接着,2018年10月举行的欧洲肿瘤医学协会会议(ESMO 2018)上,一项关于larotrectinib治疗涵盖24种独特肿瘤类型NTRK融合成人及儿童患者的临床数据显示:总缓解率:80%、部分缓解率:62%、完全缓解率:18%。在2019年1月18日,NCCN发布的非小细胞肺癌指南中,拉罗替尼(Larotrectinib)被推荐作为 NTRK 基因融合阳性转移性 NSCLC 患者的一线治疗选择。
看到这里,相信大家也有点理解了,拉罗替尼为什么被大家称为“抗癌神药”,它所公布的试验数据意味着:不管什么年龄、什么癌种(组织/细胞/部位),只要基因检测发现有NTRK基因融合突变,就可以使用拉罗替尼进行治疗。是不是听起来就让人热血沸腾?如果说,ALK突变是“钻石突变”,那NTRK融合突变也能算的上是“铂金突变”了吧?
恩曲替尼(Rozlytrek®、entrectinib)
“恩曲替尼”是在文章刚开始就提到的,2019年6月18日,罗氏宣布,日本厚生劳动省(MHLW)已批准Rozlytrek®(entrectinib,恩曲替尼)用于治疗神经营养性酪氨酸受体激酶(NTRK)融合阳性的晚期复发性实体瘤的成人和儿童患者。Rozlytrek®是第一个在日本被批准的、针对NTRK基因融合突变的实体瘤患者的靶向抗肿瘤药物。它的治疗范围非常之广,有:胰腺癌、甲状腺癌、唾液腺癌、乳腺癌、结肠直肠癌和肺癌等。从全球来看,Rozlytrek®是继拉罗替尼之后,又一个获批的泛癌种NTRK融合的广谱抗癌药。
本次Rozlytrek获批的支撑数据包括关键临床II期STARTRK-2、临床I期STARTRK-1、临床I期ALKA-372-001试验,以及面向儿科患者的临床I/II期STARTRK-NG试验。
在关键临床II期STARTRK-2试验中,结果显示超过50%的NTRK基因融合阳性的实体瘤患者肿瘤缩小,客观缓解率 (ORR) 为56.9%。在10种不同的癌症类型中都有客观反应,中位缓解持续时间(DoR)为10.4个月 ,其中包括基线有或无中枢神经系统转移的患者。重要的是,对于已经发生脑转移的患者,恩曲替尼的颅内ORR也达到了54.5%。在STARTRK-NG研究中,Rozlytrek也让NTRK基因融合阳性的儿童和青少年患者肿瘤缩小,其中包括有原发性中枢神经系统肿瘤的患者。
混世魔王”卡博替尼
卡博替尼目前已获FDA审批的适应症有4个:
1.播散至身体其他部分、转移的甲状腺髓样癌。
2.既往接受过抗血管生成治疗的晚期肾癌。
3.晚期肾细胞癌一线治疗。
4.复发难治的晚期肝细胞癌。
根据目前公布的靶点来看,卡博替尼覆盖的靶点挺多,有:MET、VEGFR1、VEGFR 2、VEGFR 3、ROS1、RET、AXL、NTRK、KIT等,可以作为备选。
瑞戈非尼
美国FDA批准瑞格非尼:
1.用于不能通过手术切除以及使用其它已上市药物治疗无效的晚期胃肠道间质瘤(GIST)患者。
2.用于治疗不可手术的肝细胞癌的治疗。
3.用于标准化疗失败的转移性结直肠癌患者。
根据目前公布的靶点来看,瑞戈非尼覆盖的靶点也挺多,有:RAF、KIT、RET、PDGFR、FGFR2、VEGFR1、VEGFR2、VEGFR3、TIE2、NTRK等,也可以作为备选。
处于临床研究阶段的类似药物也非常之多,部分适应症为“实体瘤”的药物基本信息见下表:
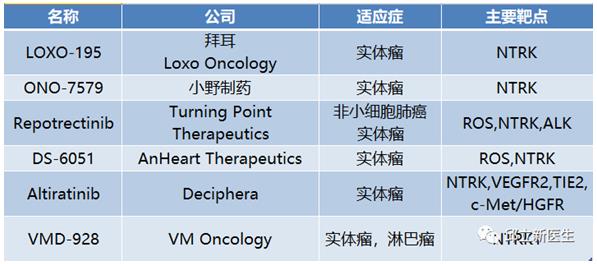
此表只列举了一部分,国内外还有其他一些公司的药品也正在研究之中,所以在有余力的情况下,邱医生还是建议患者尽量做尽可能全面的基因检测,毕竟,多一个“朋友”就多一条路嘛
好啦,关于NTRK的干货就介绍到这啦,下面是例行的福利时间,关于临床研究,不用我再多说了吧?赶快拿出你们的小本本记下来~~~
相关临床试验
试验题目
晚期实体瘤或原发性中枢神经系统肿瘤儿童患者口服TRK抑制剂larotrectinib I/II期研究(研究药物在NTRK阳性儿童受试者的有效性和安全性)
适应症
NTRK融合基因阳性实体肿瘤
试验目的
本研究是验证Larotretinib在儿童肿瘤患者中的安全性。该肿瘤必须存在特定(NTRK)基因改变。研究药物限制肿瘤细胞中NTRK基因的活性而治疗肿瘤。研究的第一部分(I期)验证儿童受试者中,剂量的安全性,药物在体内的吸收和改变,对于肿瘤的作用。第二部分(II期)主要目的是药物治疗的作用及其时长。
试验设计
试验分类:安全性和有效性
试验分期:其它
设计类型:单臂试验
随机化:随机化
盲法:开放
试验范围:国际多中心试验
入选标准
1 I期:在C1D1,患者从出生至21岁间,有局部晚期或转移性实体瘤或原发性CNS肿瘤,且肿瘤复发、进展或对现有治疗无应答,没有标准的或可用的系统性治愈性疗法;或:刚出生及更大的婴儿,被诊断为恶性肿瘤且已有记录证实NTRK融合基因,肿瘤已进展或对现有疗法无应答,且无标准的或可用的治愈性疗法。或:研究者认为通过损伤外形手术或截肢才能实现完整手术切除的局部晚期IFS患者。
2 I期剂量递增队列已完成入组。
3 期剂量扩展:除上述入选标准外,有资格入组本队列的患者必须是有记录证实NTRK融合基因的恶性肿瘤患者,IFS、CMN或SBC患者除外。入组本队列的IFS、CMN或SBC患者需有通过FISH或RT-PCR检测出ETV6重排或通过NGS检测出NTRK融合的证据。
4 II期:-C1D1时刚出生及更大的患有局部晚期或转移性IFS的婴儿患者,局部晚期IFS患者需经研究者判断后认为通过损伤外形手术或截肢方可达到完整的手术切除。或:C1D1时刚出生至21岁的局部晚期或转移性实体瘤或原发性CNS肿瘤患者,肿瘤已复发、已进展或对现有疗法无应答,并且无标准的或可用的全系统性治愈性疗法,已证实NTRK融合基因(或为IFS、CMN或SBC时有通过FISH或RT-PCR证实ETV6重排或通过NGS证实NTRK融合基因)(通过CLIA或其他类似认证实验室常规进行的分子检测确定)。NTRK融合基因阳性良性肿瘤患者也有入组资格。或:(包括扩展阶段)肿瘤诊断为儿童患者的典型组织学类型和NTRK融合基因的21岁以上的潜在患者,在当地研究中心的研究者与申办者的医学监查员进行讨论后可考虑入组。
5 原发性CNS肿瘤或脑转移患者
6 Karnofsky(≥16岁)或Lansky(<16岁)体力状态评分至少为50
7 具有足够的血液学功能
8 肝肾功能正常
相关临床试验
试验题目
NTRK融合基因阳性肿瘤患者口服TRK抑制剂Larotrectinib II期篮式研究(研究药物在NTRK阳性成人和儿童受试者的有效性)
适应症
NTRK融合基因阳性实体肿瘤
试验目的
这项研究是为了验证不同类型的肿瘤对Larotrectinib的疗效。这些肿瘤必须存在一种特定的基因变化(NTRK1, NTRK2或NTRK3)。Larotrectinib是一种试验性的药物,可以阻止这些NTRK基因在癌细胞中的作用,因此可以用来治疗肿瘤。
试验设计
试验分类:安全性和有效性
试验分期:II期
设计类型:平行分组
随机化:随机化
盲法:开放
试验范围:国际多中心试验
入选标准
1 通过分子学方法检测出NTRK1、NTRK2或NTRK3融合基因的局部晚期或转移性恶性肿瘤。
2 受试者必须接受过适合其肿瘤类型和疾病分期的既往标准疗法,或者经研究者判断不太可能耐受相应的标准治疗或获得有临床意义的获益
3 受试者必须有至少一个RECIST 1 .1定义的可测量病灶
转自邱立新医生微信公众号
